서 론
단백질 유비퀴틴화는 다양한 세포 및 발달 과정을 조절하기 위해 진핵생물이 사용하는 중요한 번역 후 변형 과정이다[1]. 고등 식물에서 유비퀴틴화 단백질은 비생물적 또는 생물적 스트레스 반응, 호르몬 반응, 세포 주기 진행 및 세포 분화에 관여한다[2–5]. 고도로 보존된 8 kDa 단백질인 유비퀴틴(Ub)은 ATP 의존적 방식으로 Ub 활성화 효소 E1에 의해 먼저 활성화되고, Ub 접합 효소 E2로 전달된다. 그런 다음 Ub-E2 복합체는 Ub-E2에서 기질 단백질로 Ub 전달을 촉진하는 Ub-단백질 리가아제 E3에 결합하며, 이는 26S 프로테아좀에 의해 인식되고 분해된다[6]. Ub E3 리가아제는 단백질 분해 기능 이외에도 DNA 복구 및 단백질 수송과 같은 비분해성 단백질 유비퀴틴화의 기능에 대한 증거가 늘어나고 있다[7].
애기장대 유전체에는 적어도 1,400개 이상의 유전자들이 서로 다른 잠재적 Ub-E3 리가아제를 인코딩할 것으로 보고 되고 있으며[8], E3 리가아제는 두 그룹으로 분류할 수 있다. 한 클래스는 단일 서브유닛으로 작용하는 RING(Really interesting new gene)/U-BOX 형태와 HECT(Homology to E6-AP carboxyl terminus) 형태인 E3 효소들로 구성되어 있다. 다른 클래스는 SCF(Skp1- Cullin-F box)와 APC(Anaphase-promoting complex)를 포함하는 E3 효소들은 다중 소단위 복합체로 기능한다[9–11]. 애기장대에서 세 번째로 큰 유전자 패밀리를 구성하고 있는 이들은 약 469개의 RING 모티프를 포함하고 있는 E3 리가아제이다[12,13]. Cys-rich RING finger는 1990년대 초 처음으로 기술되었다[14]. RING 핑거는 모티프의 다섯 번째 위치의 Cys 또는 His 잔기에 따라 C3HC4(RING-HC)와 C3H2C3(RING-H2)의 두 가지 유형으로 나눌 수 있다[15]. 최근에 많은 애기장대 RING E3 리가아제가 옥신 신호, 앱시스산 신호, 브라시노스테로이드 반응, 종자 발아, 유묘 발달, 질소 제한에 대한 적응 경로 및 당 반응과 같은 다양한 세포 과정에 관여하는 것으로 나타났다[3,16–19]. 특히, RING 단백질들은 환경 자극에 대한 반응에서 핵심적인 역할을 한다. 예를 들어, 그들은 광형태형성, 방어 신호, 노화, 추위, 가뭄, 염분 및 삼투 스트레스에 대한 내성 기전과 관련되어 있다[2,20–22].
여기에서 우리는 탈수 스트레스 반응에 관련된 더 많은 RING finger 단백질을 알아내는데 관심이 있다. 차등유전자발현 분석자료[23]에 따라 가뭄에 반응하는 유전자 애기장대 RING Zinc Finger 1(AtRZF1)(At3g56580) 을 선정하였으며, 애기장대 유전체 서열 분석에 의하면 C3H2C3-type RING-H2 finger 유전자 그룹으로 분류된다[13]. 우리가 제공하는 증거들은 AtRZF1이 생화학적 기능으로 유비퀴틴 E3 리가아제이고, 탈수 스트레스 반응에서 보존된 RING 도메인이 AtRZF1의 생물학적 기능에 중요할 수 있음을 보여준다.
재료 및 방법
애기장대는 온도 22℃, 60% 상대 습도 및 16시간 장일조건의 생장실에서 생장시켰다. AtRZF1 T-DNA 삽입 라인인 SALK_024296(atrzf1 )은 Salk Institute의 애기장대 T-DNA 삽입 컬렉션에서 획득하였다[24]. T-DNA 삽입 동형접합 식물의 선별은 유전자 특이적 정방향프라이머 5′-TCTAGA ATGTCAAGTATTCGGAATAC-3′ 및 역방향프라이머 5′-GTCGACATAGTCAAAAGGCCATCCA C-3′(upstream and downstream, respectively)를 이용하여 중합효소 연쇄반응(PCR)을 수행하였다. PCR 산물이 생성하지 않는 식물은 T-DNA left border 특이적 프라이머 5′-GCGTGGACC GCTTGCTGCACCT-3′와 유전자 특이적 정방향 프라이머를 함께 사용하여 T-DNA 삽입 여부를 확인하였다.
식물은 2주 된 애기장대 유묘들을 400 mM 만니톨을 포함하는 용액에 담가 삼투 스트레스를 주었다. 샘플은 0, 6, 12 및 24시간 동안 삼투 스트레스를 주었으며, 각각의 샘플들은 액체 질소를 이용하여 즉시 동결하고 –80℃에서 보관하였다.
AtRZF1 cDNA를 합성하기 위해 5′-GAATTCATGTCAAGTATTCGGAATAC-3′(EcoRI site underlined) and 5′-GTCGACATAGTCAAAAGGCCATCCAC-3′(SalI site underlined) 프라이머를 이용하여 PCR을 수행하였다. PCR 산물들은 제한효소 EcoRI 과 SalI 으로 처리한 후, pMAL P2x vector(New England BioLabs, USA)에 클로닝하였다. 이 플라스미드는 대장균 BL21에서 발현시켜, 아밀라아제 레진(New England BioLabs)을 이용하여 친화성크로마토그래피 통해 정제하였다. In vitro self- ubiqutination assay는 Auto-ubiquitinylation kit(Enzo Life Sciences, USA)를 사용하여 진행하였다. 반응시킨 샘플들을 12% sodium dodecyl sulfate–polyacrylamide gel electrophoresis (SDS–PAGE)를 통해 분리하였고, semi-dry transfer cell(Bio-Rad, USA)을 이용하여 polyvinylidene fluoride(PVDF) membranes(Millipore, USA)으로 이동시켰다. Immunoblots은 Enzo Life Sciences product manual에 따라 anti-Ub antibody(Enzo Life Sciences)를 사용하여 진행하였다.
결 과
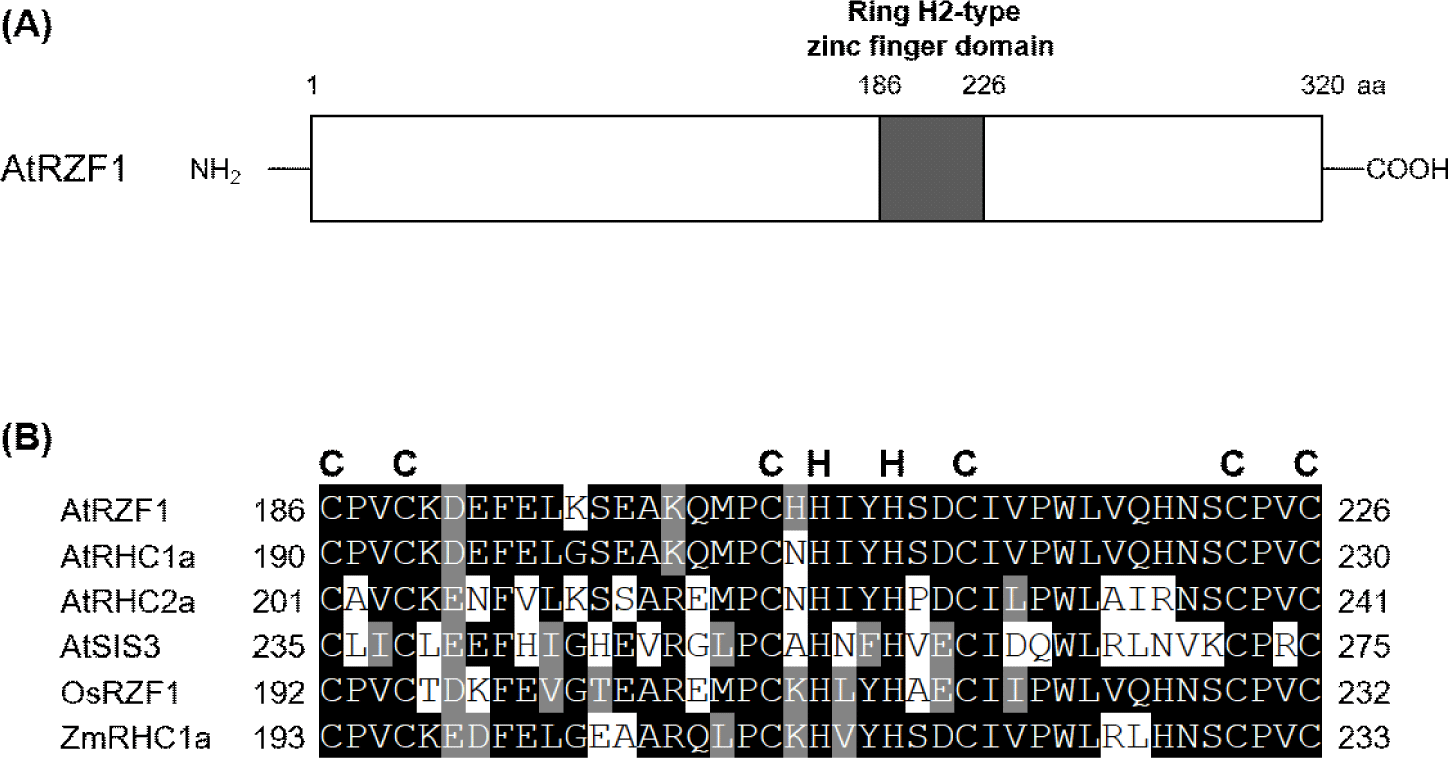
최근 전체 애기장대 유전체 염기서열 분석에 따르면 At3g56580 이 C3H2C3-type RING-H2 finger 유전자 그룹에 속하는 것으로 확인되었다[13]. At3g56580 유전자는 963 bp이며, 35.8 kDa의 분자량을 지닌 단백질로 320개 아미노산을 암호화하는 하나의 단일 오픈 리딩 프레임으로 구성되어 있다. 이 단백질에는 도메인 탐색 소프트웨어 프로그램(http://myhits.isb-sib.ch)에 의해 나타난 것처럼 zinc finger 도메인을 보유하는 것으로 예상된다(Fig. 1A). Fig. 1B에서 보이는 바와 같이, 추론된 아미노산 서열은 알려진 RING-H2 Zinc Finger 단백질 그룹과 상당한 상동성을 나타냈다. 따라서, 애기장대 At3g56580 유전자를 AtRZF1 이라고 지정하였다. Supplementary Fig. S1에서 보이는 바와 같이, 아미노산 서열 alignment 결과, AtRZF1 은 벼와 옥수수의 알려지지 않은 단백질들과 이종 상동체를 이루고 있다. 이러한 이종 상동체들은 AtRZF1 아미노산 서열과 전반적으로 36%–70%의 동일성과 43%–75%의 유사성이 관찰되었다. 애기장대 AtRZF1의 중앙영역은 기타 여러 식물의 RING 단백질과 39%–95%의 동일한 단일 RING 도메인을 포함한다. 이러한 단일 RING 도메인을 가지고 있는 단백질들의 기능은 당 신호 전달의 양성조절인자 유비퀴틴 E3 리가아제인 Sugar- insensitive 3(SIS3)를 제외하고는 잘 알려져 있지 않다[19]. Cys-X2-Cys-X14-Cys-X1-His-X2- His-X2-Cys-X10-Cys-X2-Cys 서열은 잘 보존된 41개 아미노산 RING 모티프(Fig. 1B)이며, AtRZF1은 C3H2C3-type RING-H2 단백질이다. 클러스터 알고리즘을 사용하여 아미노산 서열 그룹 간의 거리를 나타내는 계통 발생 트리를 구축하였다(Supplementary Fig. S2).
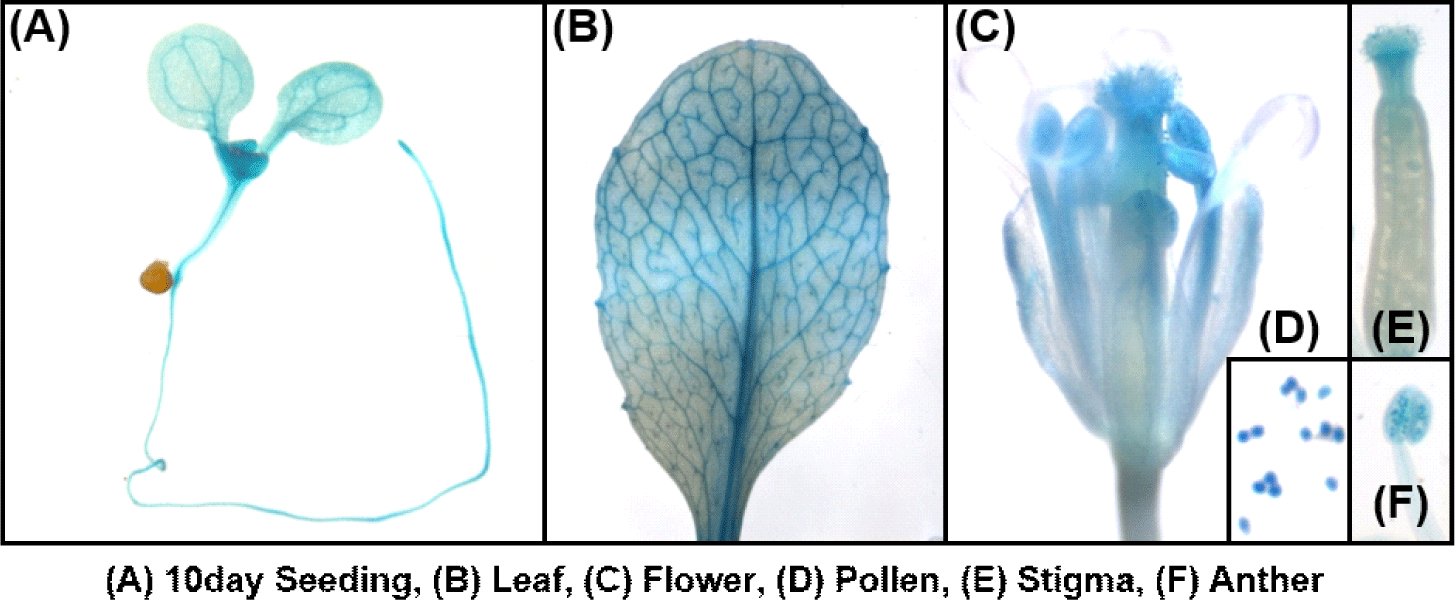
AtRZF1의 기능에 관한 단서를 얻기 위해, 1.146-kb AtRZF1 프로모터-GUS를 도입한 애기장대 형질전환 식물체들을 β -glucuronidase(GUS) 염색하여 GUS 발현 패턴을 확인하였다. 유식물체의 모든 조직(Fig. 2A), 특히 관다발계에서 강하게 발현되었으며(Fig. 2A and 2B), 꽃에서는 꽃받침과 수술대(Fig. 2C), 꽃가루(Fig. 2D), 암술머리(Fig. 2E) 그리고 꽃가루낭(Fig. 2F)에서 발현되었다[25].
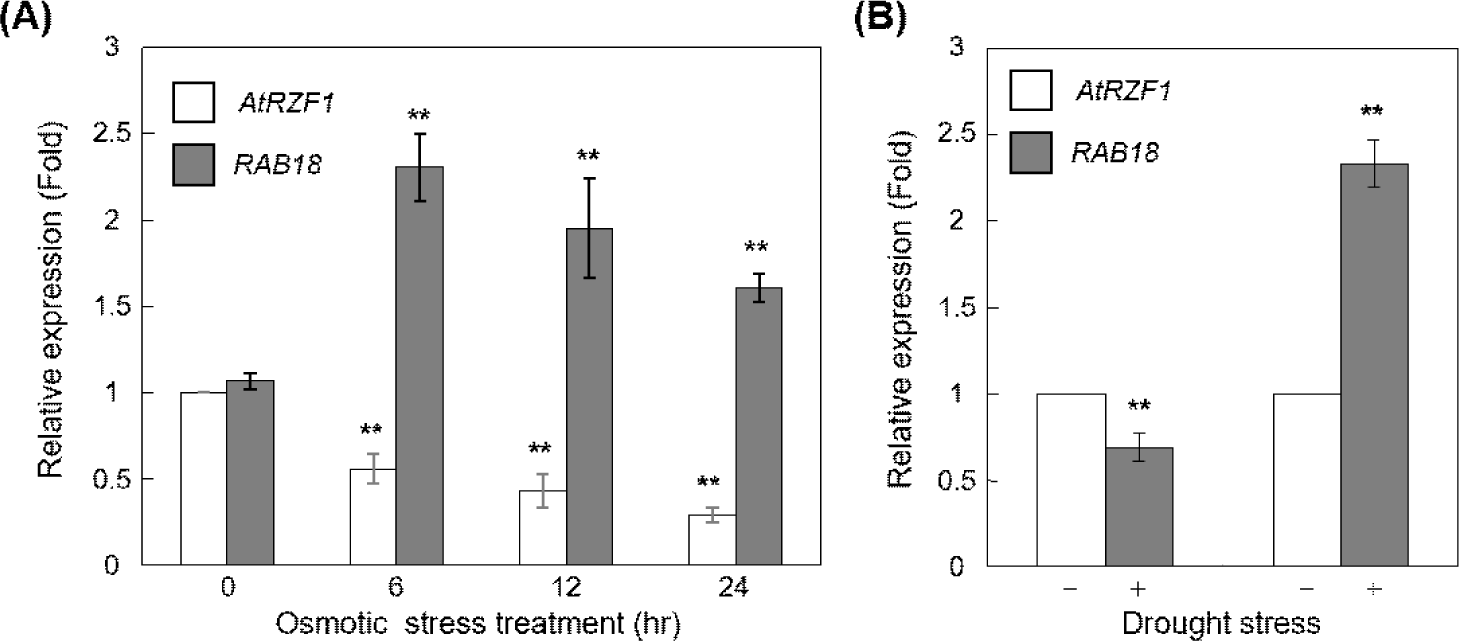
애기장대의 게놈 전체 발현 분석은 AtRZF1 의 발현이 삼투 스트레스에 의해 감소된 것으로 나타났다(http://jsp.weigelworld.org). AtRZF1의 생체 내 기능을 확인하고자 2주 된 애기장대 유묘에 삼투 스트레스를 주고 정량적 실시간 PCR을 이용하여 AtRZF1 mRNA의 발현 정도를 측정하였다. Fig. 3A에 나타난 바와 같이, AtRZF1 의 전사체 수준은 만니톨 처리 24시간 후에 3배 감소하였다. 가뭄 처리 또한 애기장대 잎에서 AtRZF1 발현의 감소되었다(Fig. 3B). 수분 부족 스트레스 처리 대조군으로 삼투 스트레스에 의해 유도되는 Responsive to ABA 18 (RAB18 )[26] 유전자를 사용하였다(Fig. 3A and 3B). 이러한 결과는 AtRZF1이 탈수 조건에 의해 조절된다는 것을 강력하게 시사한다.
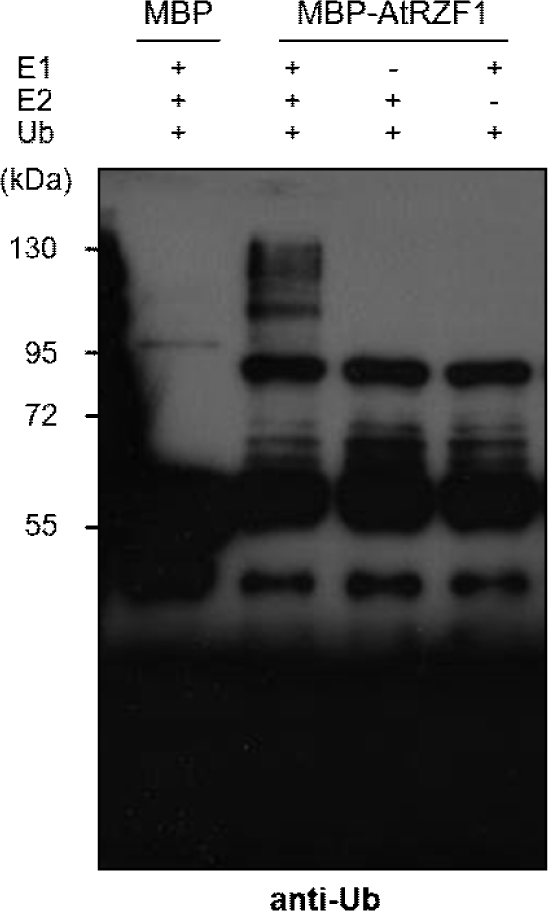
RING 도메인 단백질은 유비퀴틴화 과정에 포함된 E3 리가제의 한 유형이다[27]. AtRZF1 단백질은 C3H2C3-type RING-H2 단백질의 구성원이지만(Fig. 1B), 이전에 E3 리가아제 활성에 대해 실험된 적이 없었다[28]. 따라서, 유비퀴틴화 과정에서 AtRZF1이 E3 리가아제의 능력을 확인하는 것에 관심이 있었다. 이를 위해 AtRZF1을 in vitro 분석에 의해 E3 리가어제 활성을 확인하였다(Fig. 4). 재조합 MBP-AtRZF1 융합단백질은 대장균을 이용하여 융합된 단백질들을 생산한 후, 아밀라아제 수지를 사용하여 정제하였다(Supplementary Fig. S3). E1 및 E2가 있는 경우, 유비퀴틴화된 MBP-AtRZF1 단백질은 anti-Ub(Fig. 4) 항체를 사용한 면역블롯 분석에 의해 검출되었다. E1 또는 E2가 없는 경우, MBP-AtRZF1에서는 유비퀴틴화 활성이 관찰되지 않았다. Fig. 4에 보여주는 바와 같이, AtRZF1에 의해 유비퀴틴화된 밴드가 생성되었고, 이는 AtRZF1이 시험관 내에서 유비퀴틴 E3 리가아제 활성을 가짐을 의미한다.
생체 내 AtRZF1의 기능을 조사하고자, 35S 프로모터를 이용하여 AtRZF1 의 과발현을 유도하였다. 12개의 동형접합 계통(T3 세대)을 얻었고, 표현형 관찰을 위하여 높은 수준으로 과발현(Fig. 5A)하는 2개의 계통(OX1-1 및 OX4-2)을 선택하였다. WT과 AtRZF1 -과발현 계통을 비교한 결과, 형태학적 변경이나 성장 지연은 나타나지 않았다(Supplementary Fig. S4A). 추가적으로 애기장대에서 AtRZF1의 기능을 평가하기 위해 우리는 At3g56580 유전자에 T-DNA가 삽입된 돌연변이 SALK_ 024296을 얻었다. At3g56580 유전자의 knock-out 돌연변이체를 구하고자, exon 1에 삽입된 T-DNA의 T-DNA left border를 이용하여 RT-PCR을 수행하였다. Fig. 5A에서 보이는 바와 같이, RT-PCR 수행 결과, AtRZF1 유전자가 미발현 되는 것을 확인하였다. 해당 돌연변이는 atrzf1 로 지정하였다.
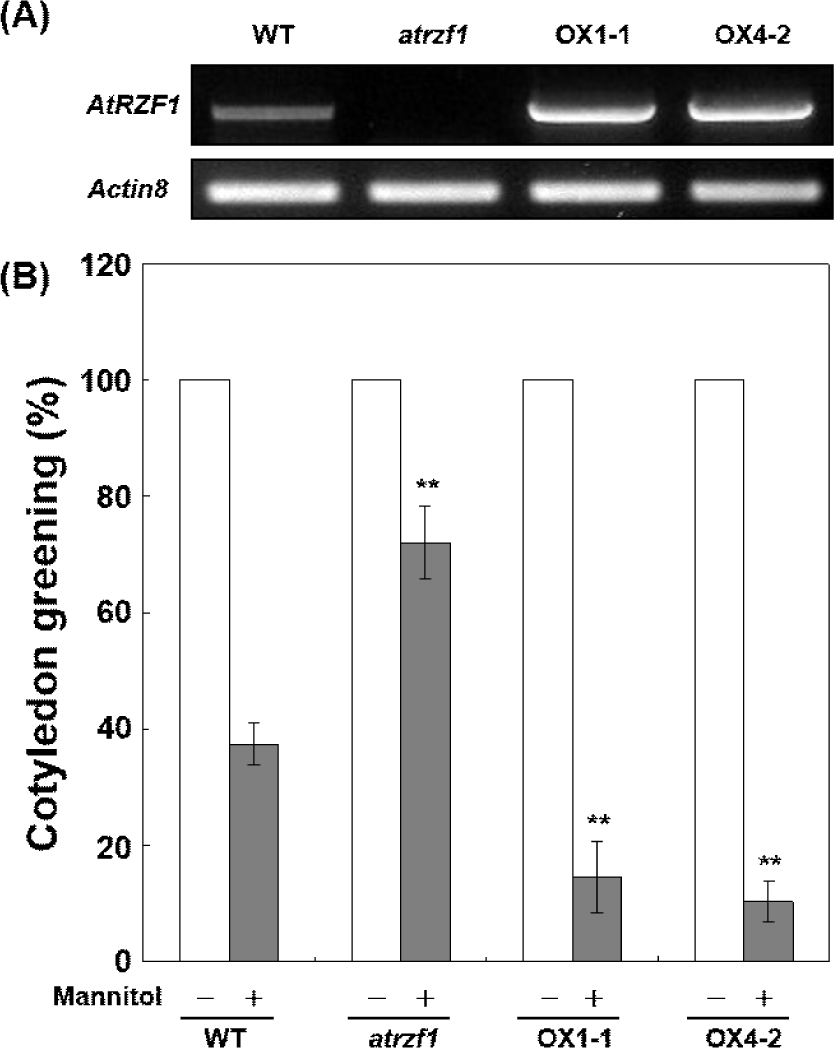
만니톨에 의해 유도되어지는 떡잎 녹화율의 피해 정도를 조사하기 위하여, AtRZF1 발현이 탈수 스트레스에 미치는 영향을 알아보았다. WT, atrzf1 및 AtRZF1 -과발현체의 종자가 0 mM 또는 400 mM 만니톨을 포함하는 MS 배지에서 발아시켰을 때, 기본 MS 배지에서 WT, atrzf1 및 AtRZF1 -과발현체 간의 발아 비율은 유사하였다(Supplementary Fig. S4A and S4B). 400 mM 만니톨이 포함된 조건에서는 발아 후 10일간 성장시켰을 때 떡잎 녹화율은 WT 잎이 약 35%이고, OX1-1 및 OX4-2 계통은 15% 미만이었다(Fig. 5B). 이에 반해, atrzf1 돌연변이체의 80%는 발아 후 10일째까지 생존하였다(Fig. 5B). 따라서, AtRZF1 -과발현체는 떡잎 발달의 관점에서 삼투 스트레스에 과민 반응을 보였고, 이는 atrzf1 돌연변이체와 AtRZF1 -과발현체가 가뭄 스트레스에 반응하여 반대 표현형을 가졌음을 보여준다.
가뭄 스트레스에 대한 반응을 추가로 알아보기 위해 식물 본엽 부분을 분리하여 수분 손실률을 측정하였다. 잎에서 수분 손실을 측정하기 위해 WT, atrzf1 및 AtRZF1 -과발현체에서 유사한 크기, 연령 및 위치의 잎을 분리하고 이전에 설명된 대로 생중량을 측정하였다[29]. 본엽 분리 후, AtRZF1 -과발현체의 잎은 주어진 조건에서 WT 및 atrzf1 식물의 잎보다 더 높은 생중량 손실이 나타났다(Fig. 6A). 그 차이는 20분 이내에 발생했으며, 이후 더 분명해졌다. 가뭄 스트레스는 또한 세포 사멸의 마지막 단계로서 원형질막 완전성의 붕괴를 수반한다. 이는 전해질 누출로 편리하게 정량화할 수 있다[30]. atrzf1 돌연변이체는 WT 및 AtRZF1 -과발현체와 비교하였을 때, 잎의 낮은 막 이온 누출 실험에서 보여지는 바와 같이 가뭄 유발 표현형이 지연되었다(Fig. 6B).
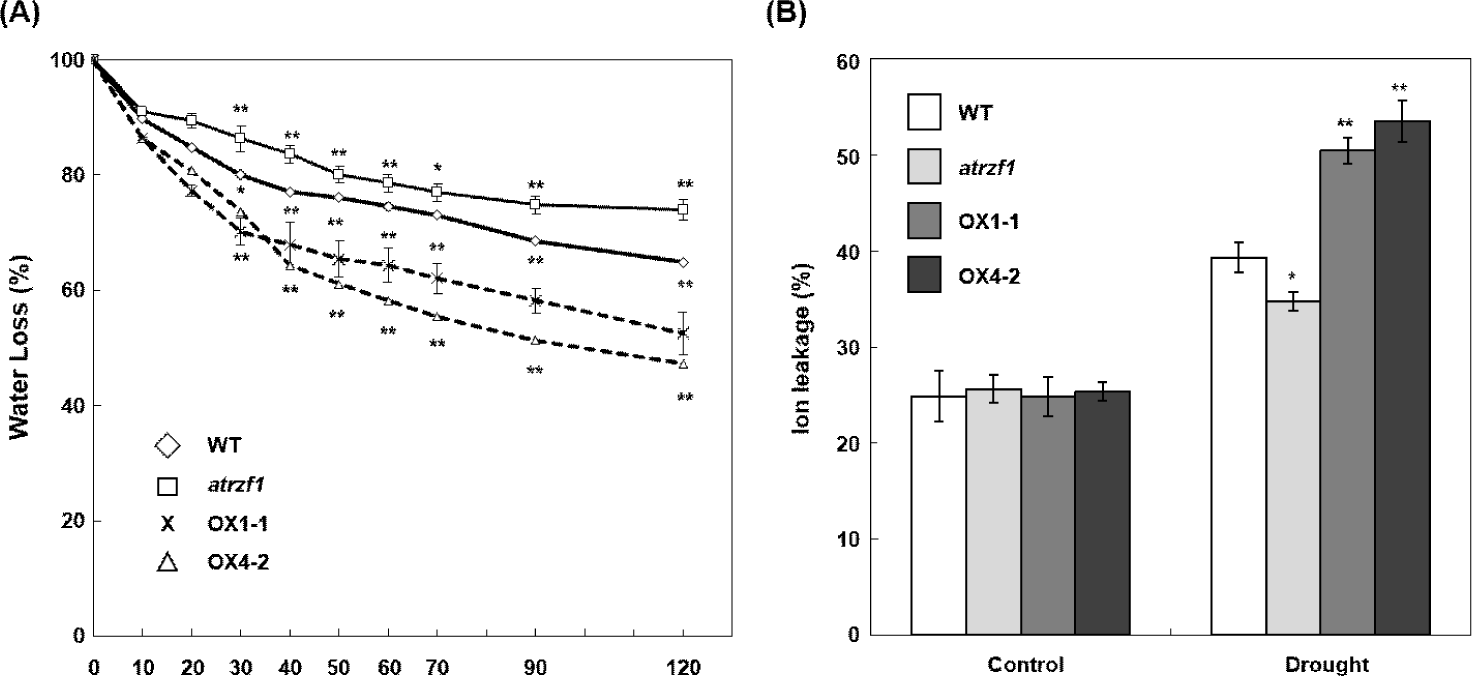
이러한 결과는 생리학적 과정에서 가뭄에 의해 유도되어지는 표현형이 WT 및 atrzf1 보다 AtRZF1 -과발현체에서 더 빨리 시작되었음을 나타낸다.
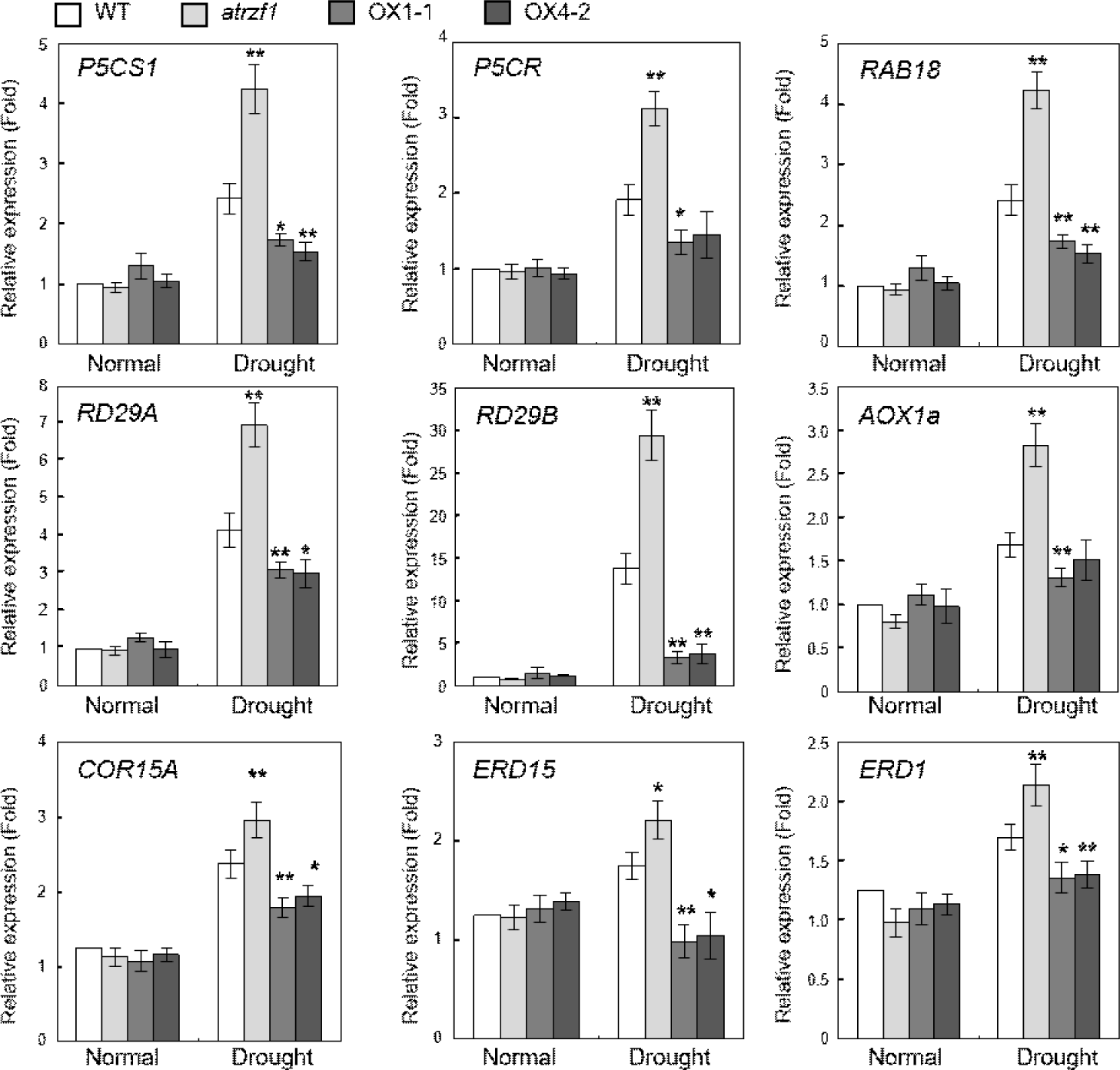
Delta1-Pyrroline-5-Carboxylate Synthase 1 (P5CS1 ), Delta1-Pyrroline-5-Carboxylate Reductase (P5CR ), RAB18 , Responsive to Dessication 29A (RD29A ), RD29B , Alternative Oxidase 1a (AOX1a ), COLD-REGULATED 15A (COR15A ), EARLY RESPONSIVE TO DEHYDRATION 15 (ERD15 ) 및 ERD1 유전자들은 스트레스에 의해 유도되어진다고 알려져 있다[31−35]. 구체적으로, P5CS1 , COR15A 및 ERD1 유전자는 ABA, 염분, 탈수 및 저온 스트레스 조건에 의해 유도되는 반면, P5CR , RAB18 및 ERD15 는 염 및 탈수 스트레스 조건에 의해 유도된다. Rd29A 및 Rd29B 는 가뭄, ABA 및 염분 스트레스 조건에서 유도된다. 또한 AOX1a 유전자는 가뭄, 빛 및 산화 스트레스에 의해 유도된다. Fig. 7은 가뭄 처리 후 P5CS1 , P5CR , RAB18 , RD29A , RD29B , AOX1a , COR15A , ERD15 및 ERD1 을 포함한 스트레스 유도성 유전자의 발현이 WT 및 atrzf1 에 비교하여 AtRZF1 -과발현체인 OX1-1 및 OX4-2에서 감소됨을 보여준다. 그러나 atrzf1 에서는 WT보다 가뭄 처리에 의해 더 많이 유도되었다. 종합하면, 우리의 스트레스 유도 유전자 발현 데이터는 AtRZF1이 가뭄 스트레스 관련 유전자 발현을 음성 조절함을 나타낸다.
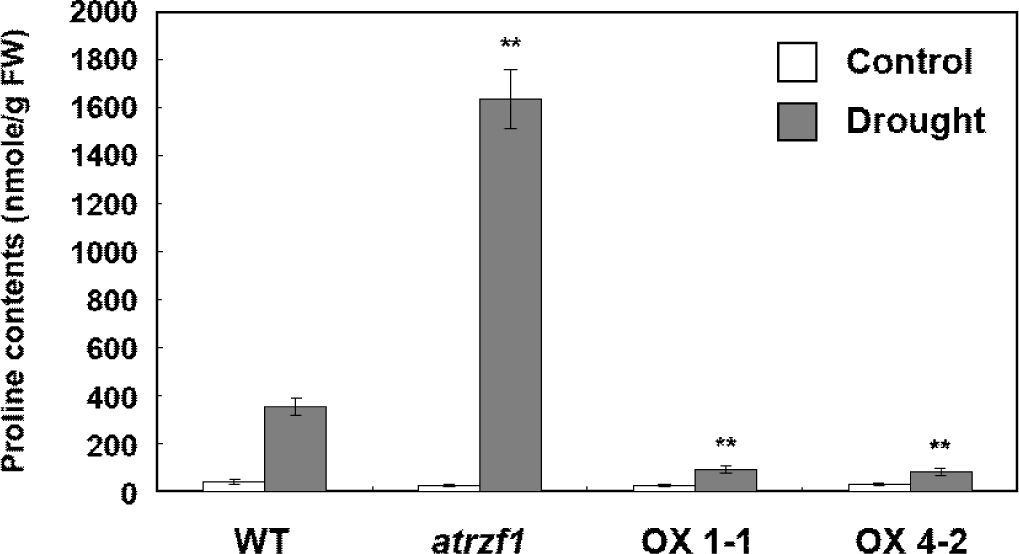
atrzf1 돌연변이체에서 P5CS1 및 P5CR 유전자의 발현이 증가했으므로, 우리는 WT 및 형질전환체의 본엽에서 프롤린 함량을 조사했다. WT, atrzf1 및 AtRZF1 -과발현체들의 프롤린 축적에 차이가 있는지 확인하기 위해 10일 간 건조 처리한 잎에서 프롤린 함량을 측정하였다. 스트레스를 받기 전에는 모든 시료에서 프롤린 함량은 비슷하게 나타났으며(Fig. 8), 가뭄 스트레스 조건에서는 WT, atrzf1 및 AtRZF1 -과발현체 간의 프롤린 함량은 상당한 차이가 관찰되었다. atrzf1 돌연변이체의 프롤린 함량은 WT 및 AtRZF1 -과발현 식물체보다 더 높은 수준으로 나타났으며, WT 식물체의 프롤린 함량은 AtRZF1 -과발현체보다 가뭄 처리에 의해 훨씬 더 많이 유도됨을 알 수 있었다(Fig. 8). 이러한 결과는 가뭄 조건에서 AtRZF1이 프롤린 생산에 음성으로 참여함을 나타낸다.
고 찰
우리는 C3H2C3-유형 RING Zinc finger 단백질을 인코딩하는 AtRZF1 유전자가 가뭄 반응에서 중요한 역할을 한다는 것을 보여주었다. 물 부족 스트레스 반응 분석 결과, atrzf1 돌연변이체가 가뭄 반응에 덜 민감한 반면, AtRZF1을 과발현하는 식물체는 더 민감하였다. 이는 AtRZF1이 초기 묘목 발달 동안 가뭄 반응을 음성으로 조절함을 시사한다.
결과적으로, 본 연구는 AtRZF1-과발현체와 atrzf1 돌연변이체 사이의 수분 손실 및 이온 누출의 뚜렷한 차이를 보여주었다(Fig. 6). 가뭄 조건에서, AtRZF1 -과발현체의 잎은 WT 및 atrzf1 돌연변이 잎과 비교하여 수분 손실 및 막 이온 누출이 크게 증가하였다(Fig. 6). P5CS1, P5CR, RAB18, RD29A, RD29B, AOX1a, COR15A, ERD15 및 ERD1 을 포함한 스트레스 유도성 유전자의 전사체 수준은 가뭄 처리 후 WT 및 atrzf1 식물보다 AtRZF1 -과발현 계통에서 감소되었다(Fig. 7). 이러한 결과는 AtRZF1이 가뭄 스트레스 반응에 음성으로 작용한다는 것을 추가로 증명한다. atrzf1 돌연변이체는 WT 및 AtRZF1 -과발현체와 비교할 때 상당한 가뭄 내성을 나타냈다. 식물 세포에 프롤린이 축적되면 삼투 스트레스로부터 세포를 보호할 수 있다[36]. atrzf1 에서 프롤린의 축적은 WT 및 AtRZF1 -과발현체에서 보다 더 많았으며(Fig. 8), 이는 AtRZF1이 삼투성 성분 조절을 통해 잎 가뭄 민감성을 유도하는 요소라고 제안할 수 있다.
RING 모티프를 포함하는 E3 리가아제는 식물 유전체에서 가장 큰 유전자 그룹 중 하나이다. 예측된 AtRZF1 단백질은 C3H2C3 유형 RING-H2 zinc finger 모티프를 보유하고 있으며(Fig. 1), 계통 발생학적 분석으로 AtRZF1이 다른 RING-H2 zinc finger 단백질 그룹 유전자와 높은 상동성을 가지는 것으로 나타났다(Supplementary Fig. S2). RING-H2 zinc finger 모티프의 경우 AtRZF1과 다른 단백질 사이의 동일성은 39%에서 95% 사이이며(Supplementary Fig. S2), 단자엽 또는 쌍자엽에서 RING-H2 zinc finger 단백질 그룹 유전자가 많이 보존되어 있음을 의미한다. 일부 RING finger 단백질은 유비퀴틴 E3 리가아제로 작용하여 유비퀴틴화/프로테아좀 과정에서 핵심적인 역할을 하는 것으로 나타났다[37]. AtRZF1은 시험관 내 분석을 사용하여 E3 유비퀴틴 리가아제 활성에 대해 실험하였다. 우리의 분석은 AtRZF1 단백질이 E1 및 E2 효소의 존재 하에서 MBP- AtRZF1 융합 단백질의 자가-유비퀴틴화의 발생에 기초하여 실제로 활성 E3 리가아제임을 입증하였다(Fig. 4).
흥미롭게도 많은 E3 유비퀴틴 리가아제는 스트레스 반응의 음성 조절자 역할을 한다. 예를 들어 HOS1(High Expression of Osmotically Responsive Genes 1)은 Inducer of CBP Expression 1(ICE1)[38]을 유비퀴틴화하여 저온 반응성 유전자의 발현을 음성으로 조절하고, DREB2A-Interacting Protein 1(DRIP1)은 Dehydration-Responsive Element Binding protein 2A(DREB2A)을 유비퀴틴화하여 스트레스 반응에서 DREB2A의 불안정화 및 하향 조절을 초래한다[39]. HSC70-Interacting Protein(AtCHIP)의 Carboxyl 말단은 Protein Phosphatase 2A(PP2A)의 A 서브유닛을 단일-유비퀴틴화하고 그 활성을 증가시키는 것으로 보고된 반면, AtCHIP -과발현 애기장대는 저온 스트레스에 대한 민감도가 증가한 것으로 나타났다[20]. 새로운 E3 리가아제인 Keep on Going(KEG) 단백질이 최근 ABA에 의해 조절되는 것으로 밝혀졌다[16]. KEG는 ABA 신호 전달의 양성 조절자인 ABA Insensitive 5(ABI5)를 상호 작용하여 분해한다. ABA는 자가-유비퀴틴화에 의한 KEG 분해를 촉진하여 KEG와 ABI5의 균형을 유지한다. 또한 여러 E3 리가아제가 비생물적 스트레스의 양성 조절자로 작용하는 것으로 나타났다. 이러한 단백질에는 ABA 신호 전달의 여러 측면에 관여하는 RING-H2 Finger A2a(RHA2a)[18] 및 ABA Insensitive RING Protein 1(AtAIRP1)[5]이 포함된다. RHA2a가 표적으로 하는 단백질은 ABA 신호 전달 경로의 음성 조절자로 제안될 수 있다. AtAIPR1의 과발현은 종자 발아 및 기공 폐쇄 동안 ABA 과민반응을 유발하여 가뭄 스트레스에 대한 내성을 초래한다.
우리의 결과에 기초하여, 우리는 AtRZF1이 유비퀴틴-프로테아좀 시스템을 통해 기질(아직 확인되지 않음)의 분해를 매개하는 E3 리가아제로 기능한다고 가정한다[16]. AtRZF1 자체가 가뭄 반응을 음성으로 조절한다는 점을 감안할 때(Supplementary Fig. S5), 우리는 AtRZF1에 의해 분해된 단백질이 수분 부족 스트레스의 양성 조절자이며, 이러한 물질을 제거하면 가뭄 반응을 활성화하는 효과가 있다고 제안한다. 따라서 식물의 가뭄 반응 네트워크를 완전히 이해하려면 AtRZF1, 표적 단백질 및 이들의 상호 작용에 대한 추가 기능 연구가 필요하다고 여겨진다.
요 약
단백질에 대한 유비퀴틴의 결합은 비생물적 또는 생물적 스트레스 반응, 면역 반응 및 아폽토시스를 포함하는 생물학적 작용을 통한 세포 기능 조절에서 근본적인 역할을 한다. 수분 결핍 반응을 통한 애기장대 RING Zinc Finger 1(AtRZF1) 단백질의 생물학적 기능을 확인하였다. AtRZF1 의 전사 수준은 가뭄 스트레스에 의하여 현저하게 감소하였다. atrzf1 돌연변이 유식물체는 초기 생장 동안 야생종에 비해 삼투 스트레스에 덜 민감한 반면, AtRZF1 과발현 형질전환체는 과민감성을 보였다. 이는 AtRZF1이 가뭄에 의해 매개하는 초기 생장 발달의 제어를 역 조절하는 것으로 나타난다. 더욱이, AtRZF1 유전자의 이소성 발현은 프롤린 함량, 수분 손실, 막 이온 누출 및 탈수 스트레스 관련 유전자의 발현을 포함하는 가뭄 민감성 매개변수에 매우 유의미한 영향을 미쳤다. AtRZF1의 식물 세포 내 기능은 E3 유비퀴틴 리가아제이며, 보존된 C3H2C3-type RING 도메인은 가뭄 반응에서 AtRZF1의 생물학적 기능에 중요할 것으로 예상된다. 또한, 이러한 결과는 E3 리가아제 AtRZF1이 초기 유식물체 생장 동안 수분 결핍 스트레스의 중요한 조절자임을 시사한다.






